Валерий Сойфер. Арифметика наследственности
Глава 18. Эволюция и молекулы
Молекулярное родство
Первые успехи эволюционной биохимии оказались многообещающими. В самом деле, что может служить более точным мерилом эволюционного сходства, чем сходство в строении молекул предка и потомка? В поисках родства изучение молекул, без сомнения, вне конкуренции. Если речь идет о белках, то совпадение последовательности аминокислот в молекулах из различных организмов — самый надежный показатель родства; если речь идет об углеводах, то совпадение в чередовании одиночных и двойных связей и т. д. Все анатомические, морфологические критерии, использовавшиеся до сих пор при установлении родства между ныне живущими существами и населявшими нашу планету в прошлом, поблекли бы и отступили на второй план перед схемами молекулярного родства. Но сегодня об этом приходится только мечтать.
Строение молекул белков и многих других органических соединений неимоверно сложно. До сих пор расшифровано ничтожно малое число таких молекул. За расшифровку почти каждой новой молекулы автор открытия удостаивался высокой научной награды — Нобелевской премии. И если эти самые первые сведения дают невероятно много для изучения эволюции, то какие же открытия ждут нас впереди!
Я приведу два примера из биохимической эволюции, чтобы стало ясно, как важны выводы этой науки.
Первый пример — структура гемоглобина. Наша кровь красного цвета. Этим она обязана одной из своих составных частей — клеткам эритроцитов. Цвет эритроцитов, в свою очередь, зависит от цвета одного из сортов молекул, входящих в их состав. Название этих молекул — гемоглобины,— наверно, известно всем. Именно гемоглобины окрашивают эритроциты в красный цвет. В каждой молекуле человеческого гемоглобина есть четыре атома железа. Вот они-то и обусловливают красную окраску этих молекул. Клетки эритроцитов в буквальном смысле нашпигованы молекулами гемоглобина: одна клетка содержит 280 миллионов молекул гемоглобина!
Роль гемоглобина трудно переоценить. Чтобы жить, надо дышать кислородом. Это банальная истина. Но если человека лишить гемоглобина, а затем поместить в атмосферу чистого кислорода, он погибнет от кислородного голодания. Он будет купаться в чистом кислороде, но не сможет им воспользоваться. Причина — отсутствие гемоглобина. Именно гемоглобин присоединяет к себе кислород и разносит его по организму. Литр безгемоглобиновой крови с трудом присоединяет три кубических сантиметра кислорода. Литр крови с гемоглобином поглощает кислорода в 70 раз больше!
Отдав кислород тканям, эритроциты проделывают другую не менее важную для жизни операцию: подхватывают «отработанные газы» (углекислый газ) и подвозят их к легким. Там ненужный углекислый газ выбрасывается и заменяется жизненно необходимым кислородом. И снова нагруженные живительным топливом — кислородом — красные кровяные клетки отправляются в путь по организму, неся с собой жизнь. И так цикл за циклом, пока работает сердце.
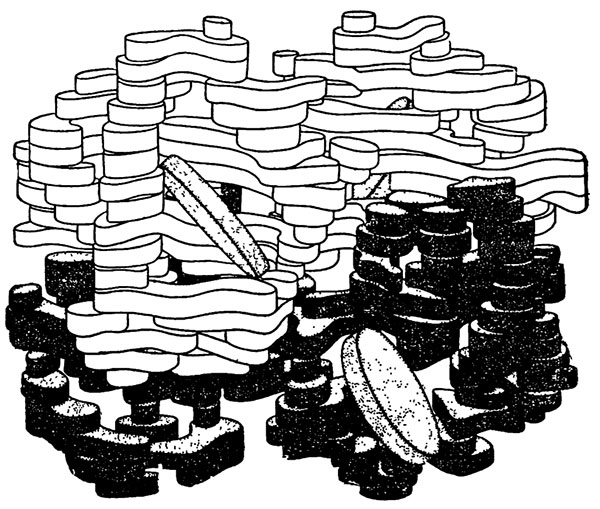
Структура гемоглобина
Гемоглобин человека состоит из четырех частей: верхняя (на рисунке светлая) половина сложена двумя одинаковыми альфа-цепями, нижняя (темная) половина составлена из двух также одинаковых бета-цепей. Альфа-цепи имеют много одинакового с бета-цепями: при наложении их друг на друга из 141 аминокислоты альфа-цепи 66 аминокислот оказываются одинаковыми и лишь 75 не совпадают. Вот оно, первое указание на родство, — почти наполовину альфа- и бета-цепи одинаковые. Считают, что предок гемоглобина мог появиться более 80 миллионов лет назад. За это время он дал начало этим двум цепям.
Семейство гемоглобинов не ограничивается этими двумя сортами молекул. Когда организм еще только зарождается, молекула гемоглобина имеет совсем другой вид. Вся нижняя половина ее составлена не из бета-цепей, а из двух так называемых гамма-цепей. Эти гамма-цепи отличаются от бета всего тридцатью семью аминокислотами. По мере развития зародыша гамма-цепи постепенно замещаются бета-цепями, и, когда кончается внутриутробный период развития, гамма-цепи уже замещены.бета-цепями. Но и это еще не все. Два процента молекул гемоглобина несут не альфа-, не бета- и не гамма-, а сигма-цепи. Сигма-цепи отличаются от бета-цепей всего десятью аминокислотами, остальные 136 аминокислот у них совпадают.
Узнав структуру альфа-, бета-, гамма- и сигма-цепей, ученые установили: наибольший путь в эволюции совершили альфа- и бета-цепи — их различие максимально. Между бета и гамма родства значительно больше: у них совпадают 109 аминокислот. Бета и сигма, можно сказать, вообще не отличаются друг от друга: вся их разница в 10 точках из 146.
До сих пор мы говорили о гемоглобинах человека. Но анализ гемоглобинов других животных дает нам еще больше сведений об эволюции. Известно, например, что морские миноги гораздо старше многих животных: когда они появились на Земле, ни обезьян, ни человека не было и в помине. Однако в подтверждение ученые приводили только косвенные факты. Самым весомым доказательством оказалась структура гемоглобина. Гемоглобин миног примитивен по своей природе — он содержит всего одну белковую цепь.
Чем дальше проникали ученые в молекулярную структуру различных гемоглобинов, тем более захватывающие открытия сопутствовали им. Общеизвестно: человек — потомок обезьяны. А как у них, наших предков, обстоит дело с гемоглобинами? Закончен анализ порядка аминокислот в бета-цепи гемоглобина гориллы, и родство выявилось. Вся разница бета-цепей гемоглобина человека и гориллы заключается в замене лишь одной аминокислоты. У человека на 104 месте стоит аргинин, у гориллы — лейцин. Остальные 145 остатков одинаковы.
Разница между свиньей и человеком существеннее: у них оказались различными 14 аминокислот. В гемоглобине лошади 18 аминокислот не похожи на аминокислоты человека.
Изучение структуры альфа-, бета-, гамма- и сигма- гемоглобинов человека, гориллы, свиньи, лошади, крупного рогатого скота выявило много молекулярных отличий. Вот тогда-то и настало время проверить правило Четверикова относительно точечных мутаций, но уже на молекулярном уровне. Да тут еще подоспели данные о составе кодонов — троек нуклеотидов, кодирующих одну аминокислоту. С этими данными в руках легко проанализировать структуру гемоглобинов. Анализ показал: первой в альфа-, бета- и сигма-цепях стоит аминокислота валин. В гамма-цепи она заменена глицином. В этом месте произошла точечная мутация. Стоит подставить тройку нуклеотидов, кодирующих валин и глицин, как оказывается, что их отличие всего в одном нуклеотиде: валин — УГУ, глицин — УГГ. Вот уж поистине точечная мутация! Аминокислоты, стоящие на втором месте, во всех цепях одинаковы — гистидины. В третьем положении в гамма-цепи опять мутация, и опять точечная, — лейцин заменен фенилаланином: УУГ на УУУ. Снова правило Четверикова подтверждается. На четвертом месте мутация произошла в альфа-цепи, там треонин заменен серином. Подставим кодоны: серии УЦЦ, треонин АЦЦ. Опять отличие всего в одном нуклеотиде. Дальше можно не продолжать. Подавляющее большинство замен, не говоря уже о расположении мутаций, точечные.
Так молекулы подтвердили справедливость предположения, высказанного С. С Четвериковым: эволюция осуществляется за счет точечных мутаций.











